SIBO: bacteriële overgroei in de dunne darm mogelijke oorzaak van aanhoudende klachten
Het menselijk maag-darmkanaal speelt een belangrijke rol in onze algehele gezondheid. Het is de plek waar voeding wordt verteerd en opgenomen in het lichaam. Het is ook de plek waar een groot aantal microben leven. Dit darmmicrobioom is een zeer complex ecosysteem van organismen die met elkaar en met de mens als gastheer samenleven.
Uit onderzoek blijkt dat de verdeling van de microben in onze darmen verschilt afhankelijk van de plek in het darmkanaal [1]. Dat heeft onder andere te maken met de omgevingsfactoren in de verschillende delen van de darm, zoals de hoeveelheid zuurstof, de zuurgraad, de darmpassage tijd ter plaatse en de beschikbaarheid van voedingsstoffen.
In de dunne darm, waar de pH waarde laag is, er veel zuurstof is en een overvloed aan beschikbare en eenvoudig te metaboliseren voedingsstoffen is, zijn er in verhouding weinig bacteriën aanwezig. De bacteriën die aanwezig zijn behoren vooral tot de phyla (families) Proteobacteriën, Streptococcus spp. en Bacteroidetes.
Verreweg de meeste microben leven in de dikke darm, waar de zuurgraad hoger is, terwijl de hoeveelheid zuurstof en snel verteerbare voedingsstoffen laag is. Je treft hier vooral bacteriën aan uit de families Firmicutes en Bacteroidetes, maar ook melkzuur producerende bacteriën zoals Lactobacillen en Bifidobacteriën.
De samenstelling van het darmmicrobioom (in de dunne en in de dikke darm) kan verstoord raken. Een SIBO is een voorbeeld van een verstoord darmmicrobioom.
In dit artikel kijken we dieper naar wat een SIBO precies is, waar je het aan herkent en welke therapeutische mogelijkheden er zijn binnen de orthomoleculaire praktijk.
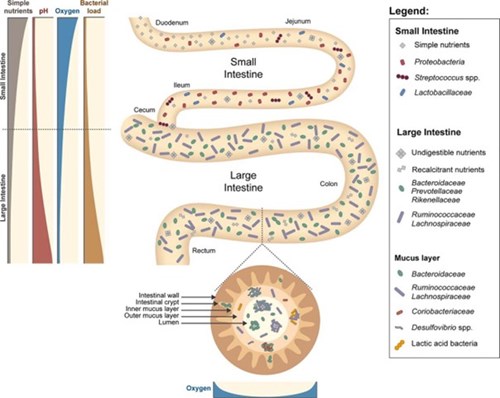
Afbeelding 1: Verdeling van aantal bacteriën en bacteriële families doorheen het darmkanaal.
Uit: Pereira FC, Berry D. Microbial nutrient niches in the gut. Environmental Microbiology. april 2017;19(4):1366–78.
Wat is een SIBO?
De afkorting ‘SIBO’ staat voor small intestinal bacterial overgrowth. Deze definitie is tot stand gekomen in de jaren ‘60 en ‘70 van de vorige eeuw toen de focus van het wetenschappelijk onderzoek rondom de klachten die met een SIBO worden geassocieerd vooral lag op de hoeveelheid bacteriën ter plaatse in de darm. Recent onderzoek doet de vraag rijzen of een SIBO ook niet mede een verstoring omvat van (uitsluitend) de samenstelling van de microben in de dunne darm [2].
Een SIBO kan gepaard gaan met een groot scala aan klachten. De meest in het oog springende klachten zijn buikklachten zoals een opgeblazen gevoel, winderigheid, buikpijn en -ongemak, chronische diarree (al dan niet vetdiarree, ook wel steatorroe of steatorrhoea genoemd). Daarnaast kan sprake zijn van malabsorptie van de vetoplosbare vitaminen A, D en E en een gebrek aan nutriënten zoals vitamine B12 en ijzer [2].
Hoe wordt de diagnose van SIBO gesteld?
De gouden standaard om een SIBO vast te stellen is het op kweek zetten van een aspiraat dat men via een enteroscopie heeft weggehaald uit het jejunum, om vervolgens het aantal bacteriën te tellen. Dit is een zeer invasieve methode die weinig wordt toegepast [3].
In de praktijk maakt men vooral gebruik van een waterstof- en/of methaangas ademtest conform de aanbevelingen van de North American Consensus uit 2017 [4]. In deze test krijgt de cliënt, na de nodige voorbereidingen, een oplossing te drinken van glucose of lactulose. Hierna meet men via ademtesten op verschillende tijdstippen de hoeveelheid waterstofgas en/of methaangas die de cliënt uitademt. Darmmicroben scheiden deze gassen uit na fermentatie van de ingenomen suikers. Afhankelijk van het tijdstip waarop een toename wordt gezien van deze gassen stelt men al dan niet een SIBO vast. Daarbij maakt men onderscheid tussen een SIBO van waterstofgas producerende bacteriën (H-SIBO) en een SIBO van methaangas producerende bacteriën (M-SIBO). Ook deze ademtesten zijn niet zonder controverse. Precieze diagnostiek is in het geval van SIBO dus niet eenvoudig. Diagnostische testen zoals de ademtest moeten steeds gecombineerd worden met het klinisch beeld van de cliënt en het inventariseren van risicofactoren. Een uitgebreide anamnese staat dus centraal.
Oorzaken van bacteriële overgroei in de dunne darm
Het lichaam heeft een groot aantal fysiologische werkingsmechanismen die moeten voorkomen dat het darmmicrobioom verstoord raakt en een SIBO mogelijk wordt. Welke dit zijn bespreken we hierna. Een verstoring in één of meerdere van de werkingsmechanismen staan aan de basis van het ontwikkelen van een SIBO. Bij een cliënt met een SIBO is het dus belangrijk dat je deze werkingsmechanismen checkt en, indien aan de orde, verbetert.
1. Een tekort aan maagzuur
Een gezonde maag heeft als gevolg van de hoeveelheid maagzuur die het produceert een zuurgraad van ongeveer 1,8. Deze zure omgeving is een van de eerste lichaamsbarrières tegen pathogenen. Een gebrek aan maagzuur vermindert dit afweermechanisme en maakt het mogelijk dat het microbioom in de darmen verstoord raakt doordat pathogenen het maagmilieu overleven en kunnen verder reizen naar de dunne darm.
Een gebrek aan maagzuur, bijvoorbeeld door het gebruik van een maagzuurremmer, kan er voor zorgen dat de zuurtegraad van de maag stijgt tot wel 7 [5]. In een meta-analyse uit 2016 is gekeken naar de relatie tussen het gebruik van een maagzuurremmer en het ontwikkelen van een SIBO. De onderzoekers concludeerden dat het gebruik van een maagzuurremmer een risicofactor kan zijn voor het ontwikkelen van een SIBO [6]. In recent, kleinschalig onderzoek onder 21 mensen met een functionele dyspepsie bleek een groot deel van hen (71,4%) te kampen met een SIBO [7].
2. Een verstoord mondmicrobioom
De mond bevat een eigen microbioom, het mondmicrobioom. Elke slikbeweging zorgt voor translocatie van mondmicroben naar het maag-darmkanaal. Als deze microben dan in de maag niet tegengehouden worden door de zuurtegraad aldaar, dan komen deze microben de dunne en dikke darm in.
Pathogene bacteriën uit de mond zoals Enterobacteriaceae (met name Klepsiella), Escherichia-Shigella en Clostridium perfringens zijn in staat zo het darmmicrobioom negatief te beïnvloeden en een SIBO te veroorzaken [8].
3. Dysfunctionele darmreiniging en vertraagde darmtransit
De darm stuwt de voedselbrij door het darmkanaal richting de anus. Om ervoor te zorgen dat er geen voedselresten achterblijven in het darmkanaal is de darm uitgerust met het migrerend motorcomplex (MMC). Dit MMC is een speciaal motiliteitspatroon van de maag en dunne darm dat de dunne darm schoon houdt en voorkomt dat daar een ongewenste wildgroei aan bacteriën kan ontstaan. Een niet goed functionerend MMC is geassocieerd met het ontwikkelen van een SIBO [2]. Factoren die de werking van het MMC verstoren zijn stress, kwaliteit van voeding, snelheid van eten, pathogenen en medicijnen zoals narcotica. Rustig en mindfull eten en bepaalde voedingsmiddelen zoals gember kunnen het MMC stimuleren [9,10].
In aanvulling hierop lijkt de darmperistaltiek en dus de darmtransittijd een rol te spelen bij het voorkomen van een SIBO. Hoewel er meer onderzoek nodig is, blijkt uit een observationele studie onder 78 patiënten waarbij gekeken is naar de darmtransittijd en SIBO, dat mensen met een SIBO, bestaande uit een overgroei aan methaan producerende bacteriën (M-SIBO), een vertraagde transittijd hebben in zowel de dunne als de dikke darm [11].
4. Dysfunctionele iliocecale klep
De dikke en dunne darm worden van elkaar gescheiden door middel van de iliocecale klep, ook wel de klep van Bauhin genoemd. Deze moet voorkomen dat bacteriën uit de dikke darm migreren naar de dunne darm. Hoe hoger de druk van deze klep, hoe beter hij sluit en dus hoe beter voorkomen wordt dat deze migratie van dikke darmbacteriën kan plaatsvinden.
Een onderzoek uit 2014 liet 23 deelnemers een draadloze motiliteitscapsule innemen. De iliocecale klep-druk werd vervolgend onderzocht. De deelnemers ondergingen ook een ademtest voor SIBO op basis van waterstofgas (H-SIBO). Vijftien van de 23 deelnemers scoorden positief op de ademtest. Deze deelnemers hadden ook een significant lagere druk van de iliocecale klep vergeleken met de deelnemers met een negatieve uitslag van de waterstofgas ademtest voor SIBO [12]. Een dysfunctionele iliocecale klep is dus een risicofactor voor het ontwikkelen van een H-SIBO.
5. Tekort aan gal of pancreasenzymen
Bacteriën hebben, net als de mens, voeding nodig. Voeding is rijkelijk aanwezig in het darmkanaal. In de gezonde situatie wordt deze voeding in de dunne darm zo volledig mogelijk verteerd en opgenomen in de bloedbaan met uitzondering van onverteerbare vezels. Zo blijft er niet veel voeding in de dunne darm achter waar de aldaar aanwezige bacteriën zich op kunnen voeden. Dit wordt anders als de spijsvertering niet goed functioneert door bijvoorbeeld een gebrek aan gal en/of pancreasenzymen.
Onderzoek uit 2018 onder 35 patiënten met chronische pancreatitis en exocriene pancreasinsufficiëntie (EPI) laat zien dat in 15% van deze patiënten een SIBO aanwezig is (vastgesteld met een waterstofgas ademtest), terwijl bij de 31 gezonde deelnemers uit de controlegroep geen enkele SIBO werd geconstateerd [13]. Deze uitkomst is consistent met andere onderzoeken. Het niet goed kunnen verteren van voeding is dus een risicofactor voor het ontwikkelen van een SIBO.
6. Anatomische obstructies in de dunne darm
Ook anatomische obstructies in de dunne darm kunnen een risicofactor zijn voor het ontwikkelen van een SIBO. Een obstructie hindert immers de normale doorstroming in de darm en ook het migrerend motorcomplex en de darmmotiliteit worden hierdoor wellicht negatief beïnvloed.
Samenvattend kunnen we stellen dat er een groot aantal werkingsmechanismen is die verstoord kan raken en zo de kans op een SIBO doet toenemen. Het goede nieuws is dat veel van deze werkingsmechanismen positief te beïnvloeden zijn met voeding, fytotherapie [2] en integrale orthomoleculaire interventies.
Voedingsinterventies bij SIBO
Het allerbelangrijkste bij de aanpak van een SIBO is het beïnvloeden van de hiervoor verantwoordelijke werkingsmechanismen of oorzaken.
Uiteraard is het belangrijk dat de cliënt een voedzaam voedingspatroon heeft dat het klachtenpatroon bij voorkeur positief beïnvloedt. De vraag hoe dit therapeutische voedingspatroon er precies uit moet zien bij een SIBO is in de wetenschappelijke literatuur nog niet beantwoord.
Een optie die regulier soms wordt ingezet is het “elemental diet”. Dit is een vloeibaar dieet dat kortdurend wordt ingezet. Het bestaat uit voorverteerde nutriënten die zo kunnen worden opgenomen in de dunne darm. Het idee erachter is dat er dan wel voeding is voor de gastheer, maar niet of nauwelijks voor de in de dunne darm aanwezig bacteriën. Het is een moeilijk vol te houden dieet, dat wel effectief kan zijn [14].
Een andere optie die wordt genoemd is het low-FODMAP dieet. FODMAP staat voor fermenteerbare oligo-, di-, monosacchariden en polyolen. Voor sommige cliënten kan dit een goede kortdurende interventie zijn, met name als er naast SIBO ook sprake is van prikkelbare darm syndroom en er heel veel klachten zijn. Er is echter onvoldoende wetenschappelijk bewijs voor de effectiviteit van het low-FODMAP dieet bij SIBO [14].
Er is eveneens wetenschappelijk bewijs voor het zogenoemde ‘SIBO-dieet’ of voor een eliminatiedieet waarbij koolhydraten worden weggelaten [15].
Kortom, je zult bij cliënten met een SIBO samen moeten vinden wat wel en niet werkt voor deze specifieke cliënt, terwijl intussen gewerkt wordt aan het optimaliseren van de hiervoor genoemde verstoorde werkingsmechanismen.
Onderbouwde phytotherapeutische of orthomoleculaire interventies bij SIBO
Bij het kiezen van interventies bij SIBO kan een onderscheid gemaakt worden tussen interventies die de eerder genoemde werkingsmechanismen aanpakken en interventies die zich rechtstreeks richten op de ontstane SIBO. Kortom, een SIBO kan je causaal alsook symptomatisch behandelen.
Voor wat betreft de interventies gericht op de verstoorde werkingsmechanismen of oorzaken, moet gedacht worden aan gember (zingiber officinale) [9,10]. Er zijn uit de praktijk veelbelovende ervaringen met gember als stimulans van zowel de maag als de motiliteit van de darmen. Meer onderzoek is echter nodig om dit te bevestigen en te bepalen wat de juiste dosering is [2], maar het toevoegen van gember in het dagelijks dieet alsook gemberthee en gemberextract is een veilige en veelbelovende interventie.
Als er sprake is van een tekort aan spijsverteringsenzymen dan is de inzet van deze enzymen ook een mooie interventie. En bij een verstoord mondmicrobioom kan gedacht worden aan orale probiotica waarmee men de mond spoelt en nadien terug uitspuugt omdat het inslikken van deze bacteriën tijdelijk de klachten kan verergeren.
Als we kijken naar interventies puur gericht op de SIBO zelf, dan zijn vooral de volgende interessant:
- Oreganum vulgare (wilde oregano olie)
Wilde oregano olie heeft antibacteriële eigenschappen en is effectief tegen verschillende pathogene bacteriën die in het darmmicrobioom worden aangetroffen [16]. In een studie uit 2014 werd voor de aanpak van SIBO een kruidenpreparaat dat bestond uit onder andere wilde oregano olie (en andere kruiden) vergeleken met het antibioticum Rifaximin. Het kruidenpreparaat bleek even effectief in de aanpak van SIBO dan het antibioticum [17].
- Lactoferrine
Er zijn nog geen wetenschappelijke studies gedaan naar het effect van lactoferrine bij SIBO. Uit studies die gedaan zijn naar het effect van lactoferrine op het ontwikkelen van het microbioom van prematuur geboren baby’s volgt echter dat lactoferrine een positief effect op het microbioom heeft.
Zo kan lactoferrine bij prematuur geboren baby’s de hoeveelheid Lactobacillen en Bifidobacteriën positief beïnvloeden en de hoeveelheid pathogene bacteriën zoals Eterobacter en Klepsiella (bekende pathogenen bij SIBO) negatief beïnvloeden [18]. Mogelijk is dit bij volwassenen ook het geval.
In elk geval zijn al heel wat mechanismen beschreven waarop lactoferrine de darmgezondheid positief kan beïnvloeden (afbeelding 2).
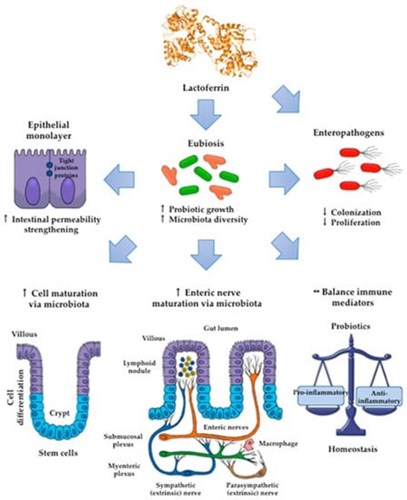
Afbeelding 2: Alle verschillende manieren waarop lactoferrine de darmgezondheid kan verbeteren.
Uit: Vega-Bautista A et.al., The Impact of Lactoferrin on the Growth of Intestinal Inhabitant Bacteria. IJMS. 23 september 2019;20(19):4707 [19].
- Bacillus coagulans
Het probioticum Bacillus coagulans kan een hele interessante interventie zijn. In een onderzoek uit 2014 werd dit probioticum in combinatie met fructo-oligosachariden (FOS) gegeven aan mensen die voor een SIBO werden behandeld met een antibioticum. Wat bleek? De mensen die naast het antibioticum ook bacillus coagulans met FOS kregen hadden een significant grotere kans op een negatieve SIBO ademtest 6 maanden na de behandeling. Ook gastro-intestinale klachten, waaronder buikpijn, namen fors af [20].
Kennis in de praktijk
Een SIBO is een serieuze aandoening met vaak forse buikklachten zoals een opgeblazen gevoel, winderigheid, buikpijn en -ongemak en chronische diarree. Tekorten in voedingsstoffen zoals vetoplosbare vitaminen, vitamine B12 en ijzer kunnen voorkomen. Het diagnosticeren van een SIBO is niet altijd eenvoudig. Onderzoek, zoals een ademtest, dient altijd gecombineerd te worden met een goede anamnese om de diagnose te kunnen stellen.
Vaak zijn er bij mensen met een SIBO verschillende werkingsmechanismen verstoord, waardoor de SIBO mogelijk is geworden. Deze werkingsmechanismen moeten aangepakt worden wil een blijvende oplossing kunnen ontstaan.
Voeding alleen is niet genoeg om een SIBO op te lossen, temeer niet nu nog niet duidelijk is welke specifieke voedingsinterventie bewezen effectief is bij SIBO. Gelukkig zijn er wel leefstijlinterventies en orthomoleculaire en fytotherapeutische interventies mogelijk die helpend zijn bij een SIBO. In combinatie met een goed voedingspatroon en het herstel van de verstoorde werkingsmechanismen zal de cliënt zich dan veel beter gaan voelen.
Bronnen:
- Pereira FC, Berry D. Microbial nutrient niches in the gut. Environmental Microbiology. april 2017;19(4):1366-78.
- Small Intestinal Bacterial Overgrowth (SIBO) - Lifestyle Matrix.pdf.
- Pitcher CK, Farmer AD, Haworth JJ, Treadway S, Hobson AR. Performance and Interpretation of Hydrogen and Methane Breath Testing Impact of North American Consensus Guidelines. Dig Dis Sci. december 2022;67(12):5571-9.
- Rezaie A, Buresi M, Lembo A, Lin H, McCallum R, Rao S, e.a. Hydrogen and Methane-Based Breath Testing in Gastrointestinal Disorders: The North American Consensus. American Journal of Gastroenterology. mei 2017;112(5):775-84.
- Mailhe M, Ricaboni D, Vitton V, Gonzalez JM, Bachar D, Dubourg G, e.a. RETRACTED ARTICLE: Repertoire of the gut microbiota from stomach to colon using culturomics and next-generation sequencing. BMC Microbiol. 24 oktober 2018;18(1):157.
- Meta-analysis proton pump inhibitors moderately increase the risk of small intestinal bacterial overgrowth.docx.
- Liu X juan, Xie W rui, Wu L hao, Ye Z ning, Zhang X yuan, Zhang R, e.a. Changes in oral flora of patients with functional dyspepsia. Sci Rep. 13 april 2021;11(1):8089.
- Barlow JT, Leite G, Romano AE, Sedighi R, Chang C, Celly S, e.a. Quantitative sequencing clarifies the role of disruptor taxa, oral microbiota, and strict anaerobes in the human small-intestine microbiome. Microbiome. december 2021;9(1):214.
- Micklefield GH, Redeker Y, Meister V, Jung O, Greving I, May B. Effects of ginger on gastroduodenal motility. Int J Clin Pharmacol Ther. juli 1999;37(7):341-6.
- Wu KL, Rayner CK, Chuah SK, Changchien CS, Lu SN, Chiu YC, e.a. Effects of ginger on gastric emptying and motility in healthy humans: European Journal of Gastroenterology & Hepatology. mei 2008;20(5):436-40.
- Suri J, Kataria R, Malik Z, Parkman HP, Schey R. Elevated methane levels in small intestinal bacterial overgrowth suggests delayed small bowel and colonic transit. Medicine. mei 2018;97(21):e10554.
- Low ileocecal valve pressure is significantly associated with small intestinal bacterial overgrowth (SIBO).docx.
- The prevalence of small intestinal bacterial overgrowth in non-surgical patients with chronic pancreatitis and pancreatic exocrine insufficiency (PEI).docx.
- Rao SSC, Bhagatwala J. Small Intestinal Bacterial Overgrowth: Clinical Features and Therapeutic Management. Clin Transl Gastroenterol. 3 oktober 2019;10(10):e00078.
- Souza C, Rocha R, Cotrim HP. Diet and intestinal bacterial overgrowth: Is there evidence? WJCC. 26 mei 2022;10(15):4713-6.
- El orégano propiedades, composición y actividad biológica de sus componentes.docx.
- Chedid V, Dhalla S, Clarke JO, Roland BC, Dunbar KB, Koh J, e.a. Herbal Therapy is Equivalent to Rifaximin for the Treatment of Small Intestinal Bacterial Overgrowth. Glob Adv Health Med. mei 2014;3(3):16-24.
- Vega-Bautista A, de la Garza M, Carrero JC, Campos-Rodríguez R, Godínez-Victoria M, Drago-Serrano ME. The Impact of Lactoferrin on the Growth of Intestinal Inhabitant Bacteria. IJMS. 23 september 2019;20(19):4707.
- Vega-Bautista A, De La Garza M, Carrero JC, Campos-Rodríguez R, Godínez-Victoria M, Drago-Serrano ME. The Impact of Lactoferrin on the Growth of Intestinal Inhabitant Bacteria. IJMS. 23 september 2019;20(19):4707.
- Evaluating the efficacy of probiotic on treatment in patients with small intestinal bacterial overgrowth (SIBO) - A pilot study.txt.